来源:赛柏蓝 作者:司徒阳明
9月10日,也就是今天,是国家局对生产工艺核查的征求意见稿接收意见的最后一天。按照征求意见稿,2016年9月10日前,意见反馈通过电子邮件反馈至食品药品监管总局药品化妆品注册管理司。药品生产企业应于2016年10月1日前完成自查并将自查情况报所在地省级食品药品监管部门。
从这个时间节点来看,这项影响国内外药企的重大政策离执行的日子并不遥远。在此之际,一个对于药企来说的,好消息也来了!
备案规范要来了
9月7日,国家食药监总局食品药品审核查验中心的一则互动消息的回复,迅速引发业界关注。
该问题是:
中药提取物干燥工艺变更
咨询内容:老师您好!如果某一品种注册工艺上是烘干(热风循环或减压干燥)现想变为喷雾干燥,属于几类工艺变更(是不是影响质量的变更)?如果把喷雾干燥的出风温度定到烘干温度是不是可以视为干燥温度不变?
回复:请咨询当地药监部门,或者等一段时间,国家局出台工艺备案政策。
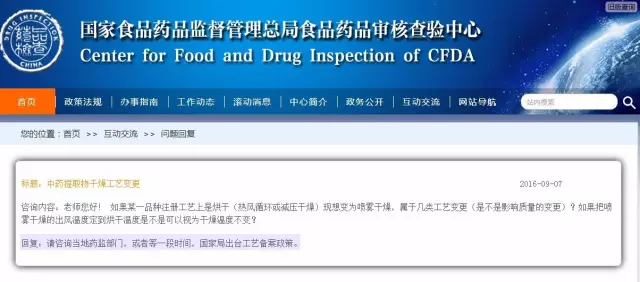
从上面的回复可以看出,等一段时间,国家局将出台工艺备案政策,未来生产工艺变更备案将会有章可循了。
生产工艺核查,影响所有药企
1个月前,8月9日,国家食药监总局发布了公开征求《关于开展药品生产工艺核对工作的公告(征求意见稿)》的意见,要求对药企的生产工艺进行核查。这对于那些,为了成本等原因造成生产工艺不规范,擅自更改生产工艺的药企来说是个绝对的震撼,是国家局为保证药品质量和药品安全出台的又一项重要政策。
但是,不可否认,也有一些企业,他们在生产工艺和注册时的工艺不符合,是有其客观的原因的。
例如一家中药企业在跟司徒君交流时就明确表示,他们的药品质量经检验是合格的,但是现在用的药材,由于质量提高了,提取物增加,已经不需要那么多投料了,所以实际生产中,工艺有所变更。但是,严格来讲,这是不符合GMP规范,在此次的生产工艺核查中,也是无法通过的。这是他们面临的现实问题。
对此,国家局也在工艺核查的征求意见稿里面提出,生产工艺的变更对质量不影响,可以提出补充申请。但是,以前,由于没有备案的规范,企业面临的实际是有点备案无门。现在,生产工艺变更是否是影响质量的变更如何备案终于要有章可循时,这对于有苦衷的企业来说是,终于找到了备案的路径了。
企业,赶紧自查工艺吧!
9月10日,是国家局对生产工艺核查的征求意见稿接收意见的最后一天。按照征求意见稿,2016年9月10日前通过电子邮件反馈至食品药品监管总局药品化妆品注册管理司。药品生产企业应于2016年10月1日前完成自查并将自查情况报所在地省级食品药品监管部门。2016年11月1日起,国家食品药品监督管理总局将组织专家对药品生产企业开展飞行检查。
对于企业来说,时间实在紧迫。
从上面的内容,我们也可以一窥国家食药监总局的监管思路,药品安全是第一位的,为了药品安全,严格监管是肯定的,但是,严格监管并不是对行业一棍子打倒,而是在保证药品的前提下,同时也照顾到企业的生产实际。
在此,笔者建议药企立马开展对生产工艺自查,以研究资料申报工艺为基础检查是否发生了工艺变更。没有变更,继续生产,资料归档作为以后检查的基础资料。
有变更的话,一定要对生产工艺进行验证,看验证结果是否会对药品质量产生影响,如果有足够信息的不影响药品质量,那么可以补充申请(备案),期间可以放心生产,不停产。但是资料一定要准备好哦。国家局的时间界节点时,仍在生产的品种2017年6月30日完成申报,其它产品12月31日完成。
有变更,验证结果有质量影响的,立即停产,重新申报。一定不要存有侥幸心里。截止时间同样是:仍在生产的品种2017年6月30日完成申报,其它产品12月31日完成。